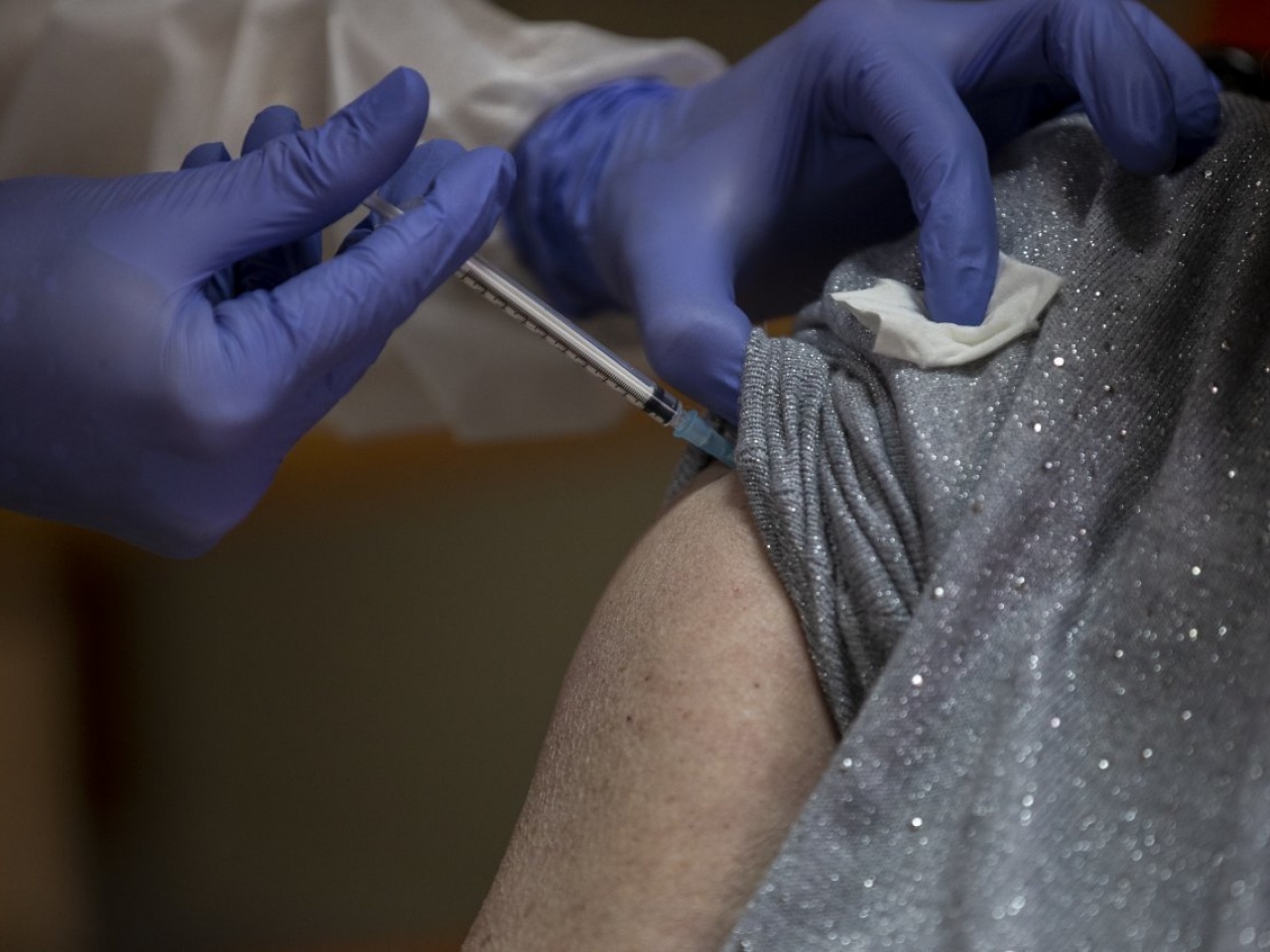
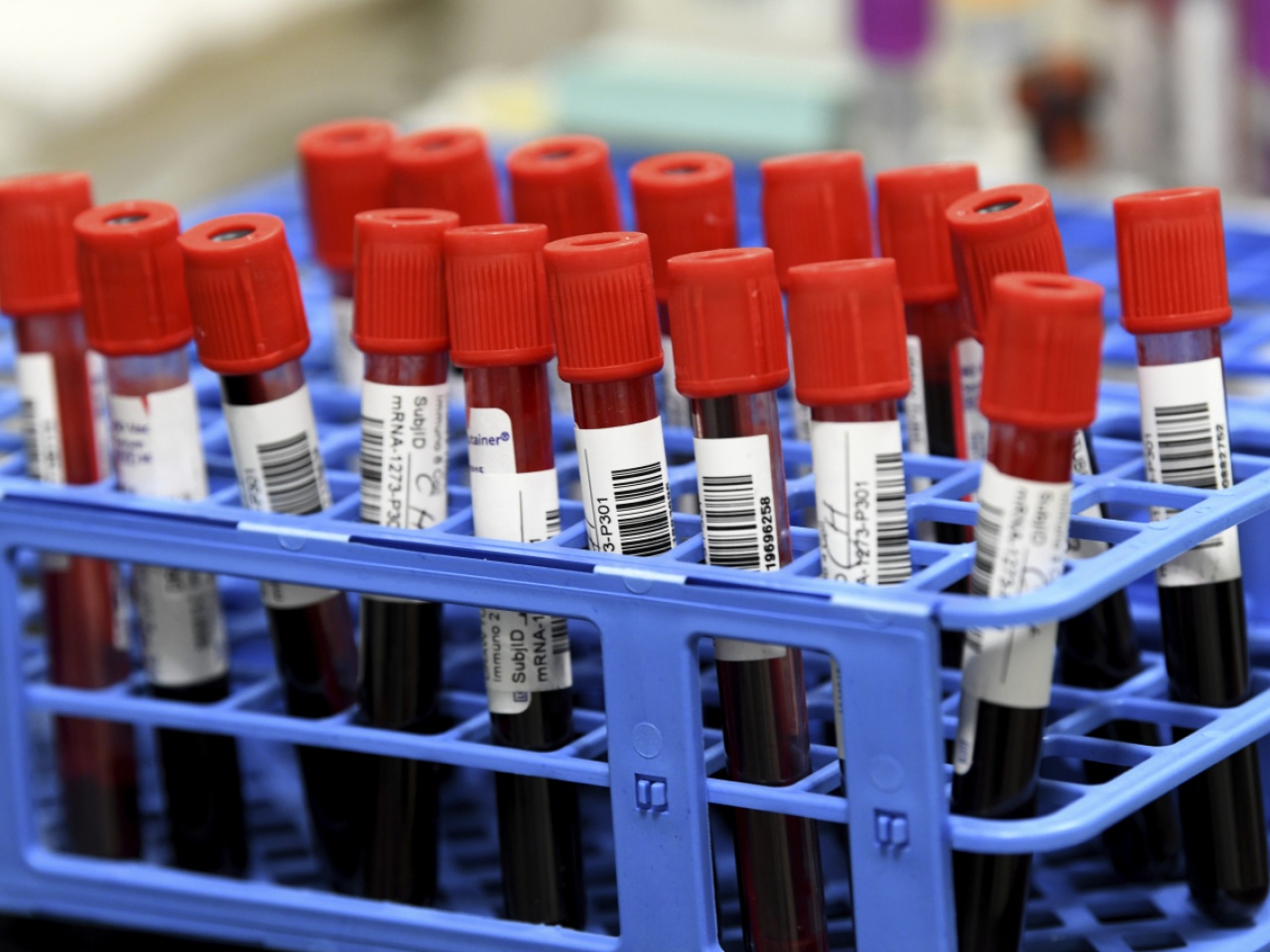
Covid, l’Oms autorizza il Comirnaty. Vaccinazioni globali al via
Con l'approvazione del vaccino Pfizer/BioNTech da parte dell'Organizzazione mondiale della sanità può iniziare la distribuzione ai Paesi in crisi
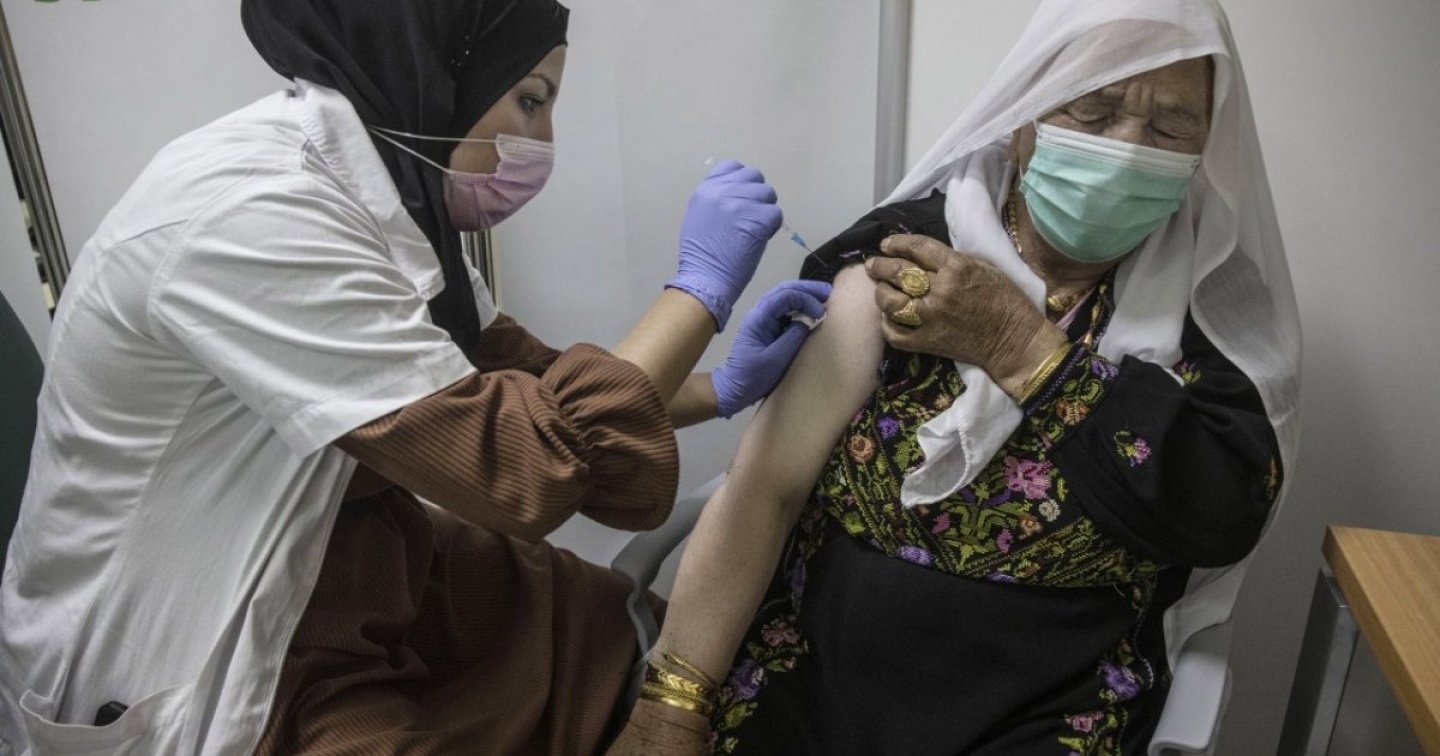
L'Organizzazione mondiale della sanità ha inserito il Comirnaty, il vaccino per il Covid-19 sviluppato da Pfizer/BioNTech, nella Emergency Use Listing, l'elenco dei prodotti terapeutici utilizzabili in caso di emergenza.
Con questa decisione i Paesi che ancora non hanno approvato questo vaccino potranno accelerare le procedure per l'importazione e la somministrazione. Ma la vera differenza riguarda il consorzio internazionale Covax di distribuzione globale del vaccino. "Questo è un passo molto positivo per garantire l'accesso globale ai vaccini. Ma voglio sottolineare la necessità di uno sforzo ancora maggiore a livello globale per ottenere una fornitura di vaccino sufficiente a soddisfare le esigenze delle persone a rischio in tutto il mondo", ha detto la dottoressa Mariângela Simão, dell'Oms. "L'Oms e i nostri partner lavorano giorno e notte per valutare altri vaccini che hanno raggiunto gli standard di sicurezza ed efficacia. Incoraggiamo un numero ancora maggiore di sviluppatori a farsi avanti per la revisione e la valutazione. È di vitale importanza che ci assicuriamo la fornitura critica necessaria per servire tutti i paesi del mondo e per arginare la pandemia".
L’Iran, il Paese più colpito del Medio Oriente, ha annunciato che importerà 16,5 milioni di dosi dal consorzio Covax, più altri 4 milioni dalla Cina.
La catena del freddo
Il vaccino Comirnaty deve essere conservato a temperature comprese tra -60°C e -90°C. Questo requisito rende il vaccino più difficile da distribuire in ambienti in cui le apparecchiature a catena ultra-fredda potrebbero non essere disponibili o accessibili in modo affidabile. Per questo motivo, l'Oms sta lavorando per supportare i Paesi nella valutazione dei loro piani di consegna e nella preparazione per l'uso, ove possibile.
Come funziona la convalida d'emergenza
La procedura per l'uso di emergenza dell'Oms riguarda la valutazione dell'idoneità dei nuovi prodotti sanitari durante le emergenze sanitarie. L'obiettivo è quello di rendere disponibili farmaci, vaccini e strumenti diagnostici il più rapidamente possibile per affrontare l'emergenza nel rispetto di rigorosi criteri di sicurezza, efficacia e qualità.
Il percorso per l'inserimento nella lista prevede una rigorosa valutazione dei dati degli studi clinici di fase II e III, oltre a sostanziali dati aggiuntivi sulla sicurezza, l'efficacia, la qualità e un piano di gestione del rischio. Questi dati vengono esaminati da esperti indipendenti e da team dell'Oms. Gli esperti delle singole autorità nazionali sono invitati a partecipare alla revisione.
L'approvazione per l'uso di emergenza è seguita dal monitoraggio dei nuovi dati e dall'approvazione ordinaria.